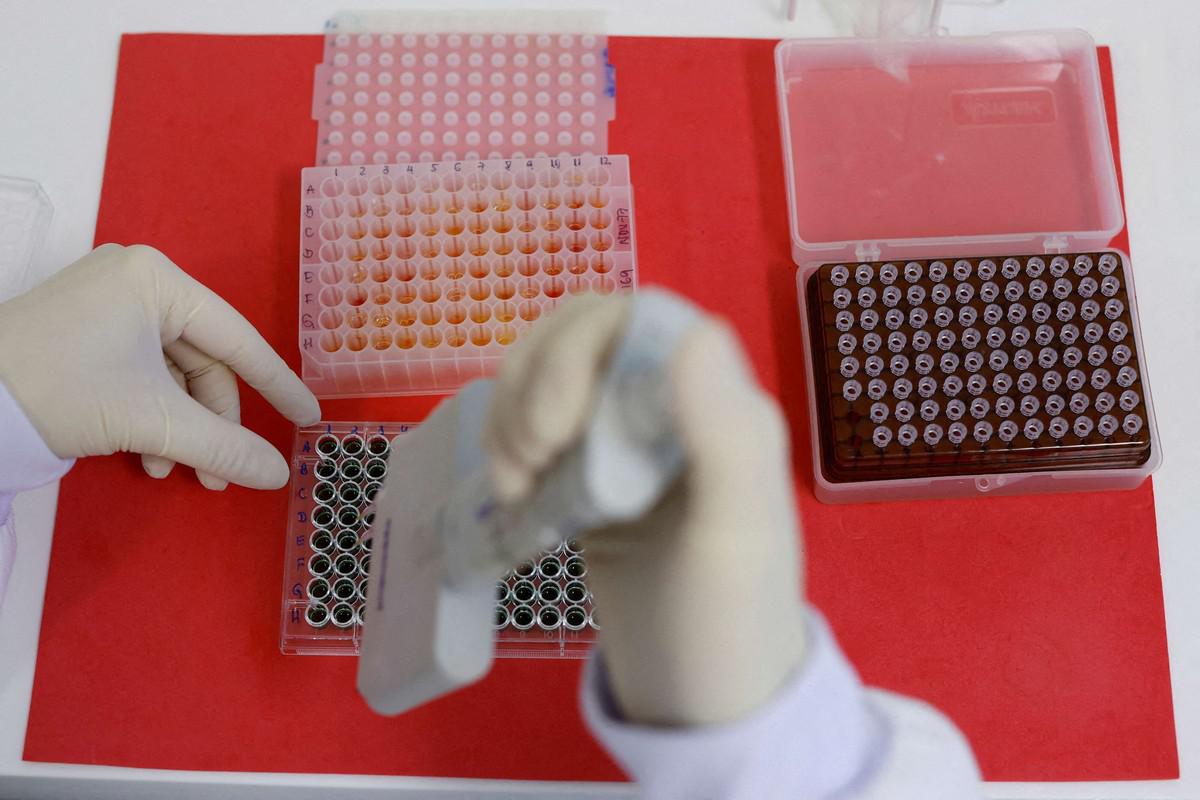
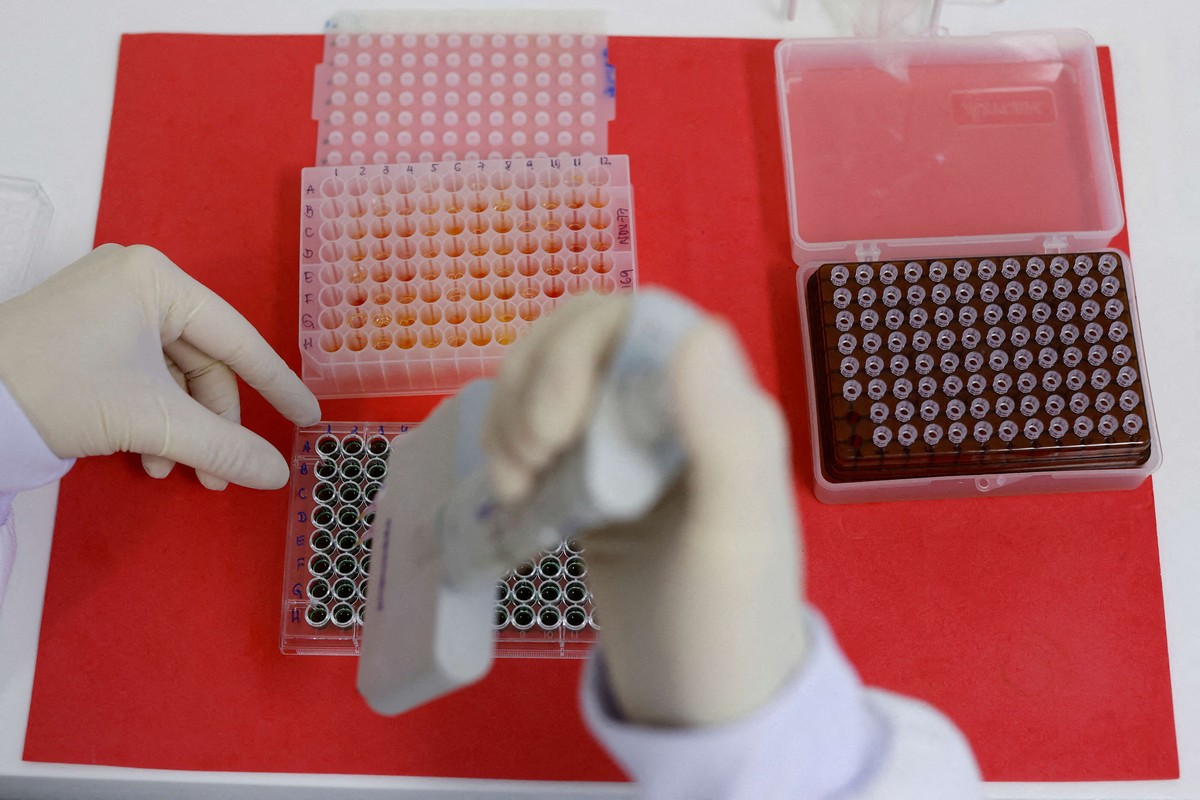
ثورة في الطب الحيوي عنوانها أجسام مضادة من الصفر بتصميم الذكاء الاصطناعي
واشنطن - في خطوة قد تُحدث تحولاً في عالم الطب الحيوي، طوّر فريق من الباحثين الأميركيين طريقة جديدة لتصميم أجسام مضادة بالكامل بواسطة الكمبيوتر، دون الحاجة إلى الحيوانات أو المكتبات العشوائية أو العينات المأخوذة من المرضى. ويعتمد الابتكار على الجمع بين الذكاء الاصطناعي المتخصص في تصميم البروتينات وتقنيات الفحص الجزيئي في الخميرة، ما يمهّد لعصر جديد في هندسة الأدوية الدقيقة.
تعتمد الطريقة على شبكة تعلم عميق تُعرف باسم RFdiffusion، وهي نسخة معدّلة من نظام تصميم البروتينات الذي يستند إلى تقنيات مشابهة لتلك التي تستخدمها أنظمة التنبؤ بالهيكل الجزيئي مثل AlphaFold. وبعد تدريبها خصيصًا على البنى المعقدة للأجسام المضادة، تمكنت الشبكة من توليد سلاسل بروتينية جديدة تشكّل مناطق الارتباط الفعالة (CDRs) التي تحدد خصوصية الجسم المضاد تجاه جزيء بعينه.
وأوضح الباحثون أن هذه المنهجية سمحت لهم بتصميم أجسام مضادة صغيرة من نوع VHH – وهي أجسام أحادية السلسلة تُستخلص عادة من الإبل – إضافةً إلى مقاطع ثنائية السلسلة (scFv) وأجسام مضادة كاملة قادرة على الارتباط بمواقع محددة (epitopes) بدقة ذرّية.
ولإثبات فعالية التصميم، اختبر الفريق أجسامًا مضادة استهدفت أربعة مواضع مرضية ذات أهمية طبية، من بينها بروتين الهيماغلوتينين لفيروس الإنفلونزا وسمّ بكتيريا Clostridium difficile.
وأظهرت صور المجهر الإلكتروني بالتبريد (cryo-EM) أن هذه الأجسام المضادة صُممت بدقة عالية، إذ تطابقت بُناها الجزيئية مع النماذج الكمبيوترية بفارق لا يتجاوز 1.5 أنغستروم، وهو ما يعادل تقريبًا دقة التصوير الذري.
ورغم أن التصاميم الأولية كانت ذات قدرة ارتباط متوسطة تراوحت بين عشرات إلى مئات النانومولات، فقد استعان العلماء بتقنية تطور موجّه تُعرف باسم OrthoRep، تتيح تسريع الطفرات وتحسين الأداء داخل خلايا الخميرة. ونتيجة لذلك، ارتفعت قدرة الارتباط إلى مستوى بضع نانومولات فقط، مع المحافظة على التخصّص الدقيق تجاه الموقع المستهدف.
وأكدت التجارب المخبرية أن أحد الأجسام المضادة المصممة ضد بروتين الهيماغلوتينين للإنفلونزا تمكن من الارتباط بالبنية الثلاثية الكاملة للفيروس في الموقع المطلوب، كما نجح جسم مضاد آخر في تعطيل سمّ بكتيريا C. difficile من خلال استهداف منطقة لم تكن قد عُرفت سابقاً بأنها قابلة للارتباط.
ويُعد هذا الإنجاز قفزة كبيرة في مجال تصميم الأدوية الحيوية. فحتى الآن، كان تطوير الأجسام المضادة يتطلب عملية معقدة تتضمن تحصين الحيوانات أو غربلة مكتبات ضخمة بحثاً عن جزيئات ترتبط بالهدف العلاجي المطلوب. وغالباً ما كانت هذه الطرق تستغرق أشهراً طويلة، وتفشل في تحديد الأجسام المضادة الأكثر دقة من حيث الموقع المستهدف. أما النهج الجديد، فيمكنه نظرياً تصميم جسم مضاد لأي موقع بروتيني معروف خلال أسابيع قليلة فقط.
نقلة نوعية لأنها تتيح لنا تصميم الأجسام المضادة من الصفر وفق الطلب
وقال أحد الباحثين المشاركين في الدراسة إن "المنصة الجديدة تمثل نقلة نوعية لأنها تتيح لنا تصميم الأجسام المضادة من الصفر وفق الطلب، مع الحفاظ على دقة هيكلية لم تكن ممكنة سابقاً إلا بعد سنوات من التجارب".
وأضاف أن الفريق يسعى الآن إلى توسيع نطاق التجارب ليشمل أهدافاً علاجية معقدة، مثل البروتينات السرطانية أو المستقبلات العصبية.
كما طور الفريق خوارزمية فرعية أخرى من نظام RoseTTAFold لتحسين دقة التحقق الكمبيوتري من التصاميم. هذه النسخة المُعدلة من الشبكة قادرة على التنبؤ بمدى نجاح الجسم المضاد المصمم في الارتباط بالهدف قبل إنتاجه فعليًا، مما يقلل من عدد التجارب غير الضرورية.
وبحسب الباحثين، فإن الجمع بين شبكتي RFdiffusion وRoseTTAFold يفتح الطريق أمام إنشاء منظومة متكاملة لتصميم واختبار الأجسام المضادة رقمياً، بدءاً من توليد البنية ثلاثية الأبعاد ووصولاً إلى تحسينها واختبارها افتراضيًا.
وتوقع محللون في قطاع التكنولوجيا الحيوية أن يؤدي هذا التطور إلى خفض كبير في تكاليف تطوير الأدوية الحيوية، التي تُقدر قيمتها السوقية العالمية بأكثر من 445 مليار دولار خلال الأعوام الخمسة المقبلة. كما قد يمكّن المنصة من التعامل بسرعة مع الأوبئة الجديدة عبر تصميم أجسام مضادة موجهة إلى بروتينات الفيروسات الناشئة خلال أسابيع قليلة فقط.
ورغم النجاح اللافت، يشير الخبراء إلى أن الانتقال من المختبرات الكمبيوترية إلى الاستخدام السريري ما زال يتطلب مراحل تقييم صارمة تشمل الفعالية داخل الجسم البشري وسلامة الاستخدام. ومع ذلك، فإن هذا العمل يمثل أول برهان عملي على إمكانية تصميم أجسام مضادة جديدة كلياً داخل الكمبيوتر، دون الحاجة لأي نموذج أولي مأخوذ من الطبيعة.
ويؤكد الباحثون أن التطور السريع في تقنيات الذكاء الاصطناعي التوليدي يمكن أن يجعل تصميم الأدوية الدقيقة عملية رقمية بالكامل، تتيح للعلماء ابتكار علاجات مخصصة بدقة متناهية لكل مريض أو لكل طفرة جينية على حدة، وهو ما قد يعيد تعريف مفهوم الطب الشخصي في العقود المقبلة.